จุฬาฯเผยผลทดลอง ‘วัคซีนโควิด-19’ ในลิงได้ผลดีมาก เตรียมส่งโรงงานผลิตทดลองในคน คาดแล้วเสร็จ พ.ย.นี้ เริ่มฉีดเฟส 1 ไม่เกินปลายปี’63
เมื่อวันที่ 12 กรกฎาคม ที่โรงพยาบาล (รพ.) จุฬาลงกรณ์ สภากาชาดไทย ศ.นพ.สุทธิพงศ์ วัชรสินธุ คณบดีคณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย และผู้อำนวยการ รพ.จุฬาฯ และพร้อมด้วย ศ.นพ.เกียรติ รักษ์รุ่งธรรม ผู้อำนวยการบริหารโครงการพัฒนาวัคซีนโควิด-19 ศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาฯ แถลงความคืบหน้าการพัฒนาและผลการทดสอบวัคซีนโควิด-19 ในลิงเข็มที่ 2 พร้อมเปิดแผนการเดินหน้าทดสอบในมนุษย์ (จิตอาสา)
ศ.นพ.สุทธิพงศ์ แถลงว่า เป็นครั้งแรกที่คณะแพทยศาสตร์ จุฬาฯ แถลงข่าววัคซีนอย่างเป็นทางการ และในวันนี้มีความชัดเจนของการดำเนินการวิจัยที่มาก โดยการระบาดโควิด-19 ทั่วโลก ที่ผ่านมา รพ.จุฬา ได้มีการรักษาผู้ป่วยโควิด-19 กว่า 200 ราย แต่เป็นการรักษาปลายน้ำ จึงคิดค้นการป้องกันด้วยวัคซีน ในความพร้อมของศูนย์วัคซีนจุฬาฯ มีทีมนักวิจัยได้พัฒนาร่วมกันมามากว่า 15 ปี ในครั้งนี้จึงมีการวิจัยวัคซีนโควิด-19
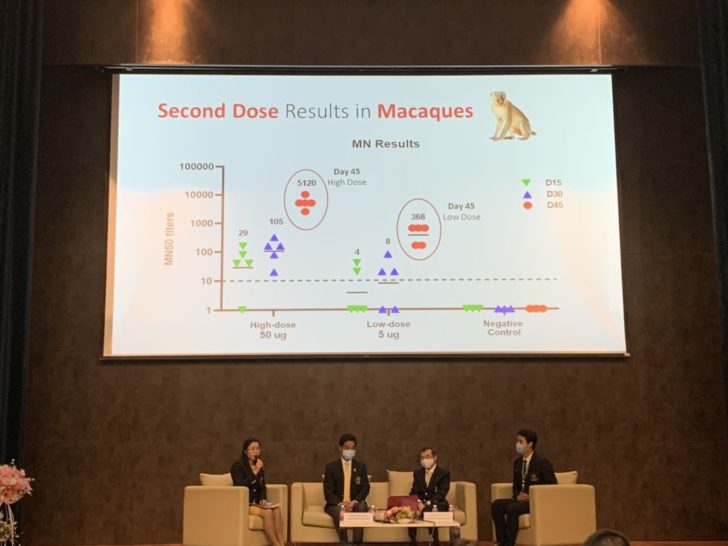
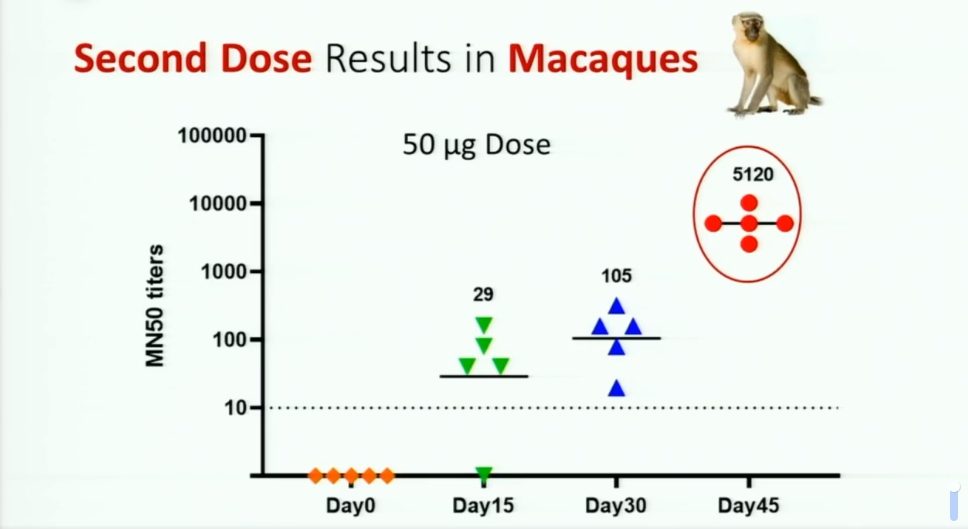
ศ.นพ.เกียรติ แถลงว่า การพัฒนาวัคซีนที่ชื่อว่า CHULA-Covid19 เป็นการพัฒนาวัคซีนชนิด mRNA โดยผลิตจากสารพันธุกรรมของเชื้อไวรัสโควิด-19 บางส่วน เพื่อผลิตใช้ในการกระตุ้นภูมิคุ้มกันชนิดแอนติบอดี้เพื่อต่อสู้กับไวรัส ก่อนหน้านี้ มีการทดลองในหนูได้ผลดีเกินคาด จึงเริ่มทดลองต่อในลิง ทั้งนี้การทดลองฉีดเข็มที่ 2 เมื่อวันที่ 22 มิถุนายน จนถึงวันนี้รวมระยะเวลากว่า 45 วัน พบว่าลิงทั้งหมด 13 ตัว ได้ภูมิคุ้มกันในระดับที่ 5,000 ไตเตอร์ (Titers) ซึ่งเป้าหมายคือ จะต้องมีภูมิคุ้มกันอย่างน้อย 1: 100 ไตเตอร์ จึงจะควบคุมเชื้อไวรัสได้ทั้งในปอดและโพรงจมูก
“ยอมรับว่าผลทดลองในลิงออกมาสวยมาก แต่ผลการพัฒนาจากการทดลองในหนูไปสูงลิง ระดับภูมิคุ้มกันตกไป 10-20 เท่า เนื่องจากขนาดตัว และสภาวะการสร้างภูมิคุ้มกันในสัตว์ที่ต่างกัน จึงคาดว่าการทดลองในมนุษย์คงลดจากลิงไปอีก 5-10 เท่า” ศ.นพ.เกียรติ กล่าวและว่า หลังจากนี้จะส่งวัคซีน 2 ตัว ที่มีสารพันธุกรรมต่างกันเล็กน้อยไปผลิตที่โรงงานเพื่อนำมาทดลองใช้ในมนุษย์ ถ้าตัวไหนผลิตได้จำนวนมาก ก็จะเลือกใช้ตัวนั้น โดยใช้ 2 โรงงาน ซึ่งได้จองเรียบร้อยแล้ว โดยกำหนดคาดว่า 2 สัปดาห์หน้าจะส่งไปยังโรงงานแรกที่สหรัฐอเมริกา เพื่อผลิตเนื้อวัคซีน mRNA คาดว่าในต้นเดือนตุลาคมนี้ จะผลิตเนื้อวัคซีนแล้วเสร็จ และโรงงานที่ 2 ผลิตตัวเคลือบ คาดว่าจะส่งไปในช่วงเดือนพฤศจิกายน และเมื่อได้วัคซีนที่สำเร็จแล้ว จะต้องนำมาฉีดทดลองซ้ำในหนูอีกครั้ง เพื่อยืนยันความปลอดภัย และเพื่อให้คณะกรรมการอาหารและยา (อย.) มีความมั่นใจ
ศ.นพ.เกียรติ กล่าวถึงการทดลองฉีดในมนุษย์ว่า ขณะนี้ยังไม่เปิดรับอาสาสมัครใดๆ เนื่องจากยังไม่ผ่านการตรวจสอบความปลอดภัยของวัคซีนจากสำนักงานคณะกรรมการอาหารและยา (อย.) แต่ในหลักการตามแผนแล้ว การทดลองในมนุษย์ระยะที่ 1 จะเริ่มในช่วงไม่เกินปลายปีนี้ ใช้อาสาสมัครทั้งหมด 150 คน แบ่งกลุ่มเป็น 2 กลุ่ม กลุ่มละ 75 คน กลุ่มที่ 1 อายุ 18-60 ปี และกลุ่มที่ 2 อายุ 60 ปีขึ้นไป ทั้งนี้จะฉีดในปริมาณวัคซีนที่ 10 ไมโครกรัม (มคก.) 30 และ 100 มคก. และระยะที่ 2 ใช้อาสาสมัคร 500-1,000 คน ใช้วัคซีนประมาณ 10,000 โดส
ศ.นพ.เกียรติ กล่าวว่า ในการทดลองฉีดในมนุษย์ของทีมจุฬาฯ ได้คิดวิธีการให้วัคซีนในมนุษย์ที่ต่างจากที่อื่น โดยระยะที่ 1 เริ่มในกลุ่มที่ 1 อายุ 18-60 ปี จำนวน 75 คน จะมีการแบ่งการฉีดกลุ่มที่ 1 จำนวน 15 คน ในปริมาณ 10 มคก. หากมีจำนวน 6 คน ที่ได้ผล ก็จะเริ่มฉีดกลุ่มที่ 2 จำนวน 15 คน ในปริมาณ 30 มคก. และกลุ่มที่ 3 จำนวน 15 คน ในปริมาณ 100 มคก. โดยใน 3 กลุ่มนี้ จะให้วัคซีนเข็มที่ 2 เพื่อการกระตุ้นภูมิคุ้มกันในปริมาณที่เท่ากับเข็มที่ 1
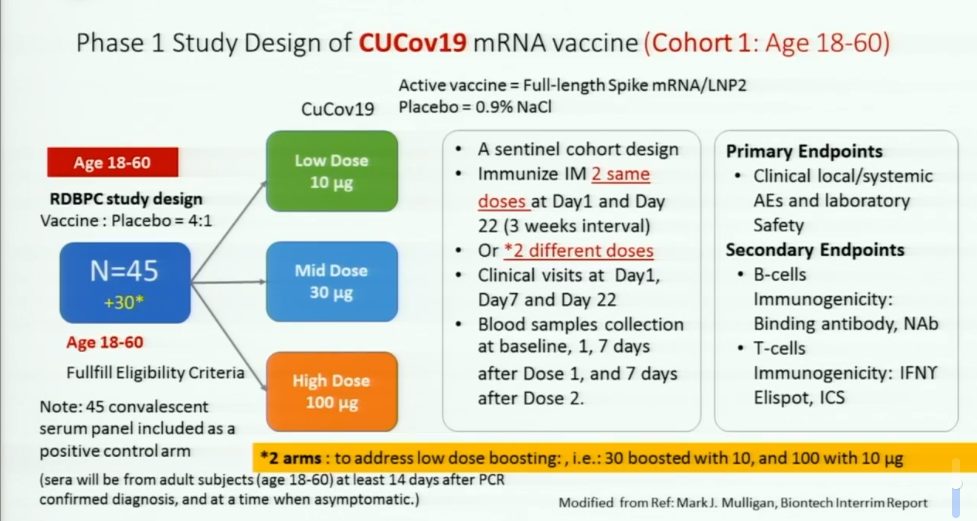
“แต่สิ่งที่แตกต่างจากที่อื่นคือ ทางทีมวิจัยได้คิดค้นว่า การทดลองเพิ่มเติมใน 2 กลุ่ม จำนวนกลุ่มละ 15 คน ที่ได้รับวัคซีนในปริมาณที่มากแล้วแต่มีการกระตุ้นด้วยวัคซีนที่น้อย จะมีการสร้างภูมิคุ้มกันได้มากเพียงใด จึงมีการทดลองในกลุ่มที่ 4 และ 5 โดยเข็มแรกจะฉีดในปริมาณที่ 30 และ 50 มคก.ตามดับ และฉีดเข็มที่ 2 กระตุ้นภูมิคุ้มกันในปริมาณเพียง 10 มคก. ในทั้ง 2 กลุ่ม เพื่อดูว่าการกระตุ้นภูมิคุ้มกันในปริมาณที่น้อยจะสามารถป้องกันเชื้อไวรัสได้มากน้อยเพียงใด ทั้งนี้ เพื่อเป็นการบริหาร ลดการใช้ทรัพยากรผลิตวัคซีนและเพื่อให้สามารถกระจายการใช้วัคซีนไปได้มากยิ่งขึ้น” ผู้อำนวยการบริหารโครงการพัฒนาวัคซีนโควิด-19 กล่าว
ศ.นพ.เกียรติ กล่าวอีกว่า ขณะนี้ทั่วโลกมีผู้พัฒนาวัคซีนชนิด mRNA ประมาณ 18 ตัว แต่มี 4 ตัว ที่ก้าวหน้ากว่าไทยอยู่ 6 เดือน แต่เป็นการใช้เทคโนโลยีที่คล้ายกันมาก ดังนั้น มีการคาดการณ์ว่า ถ้ามี 1 ตัวสำเร็จในต้นปีหน้า ถ้าหากได้การรับรองจาก อย.สหรัฐ และ อย.ยุโรป จะสร้างความเชื่อมั่นให้กับ อย.ประเทศไทย และไทยอาจจะไม่ต้องทำการทดลองในคนระยะที่ 3 เพื่อทุ่นทรัพยากรและเวลาได้ถึง 9 เดือน อย่างไรก็ตาม ขณะนี้การทดลองในมนุษย์ของไทย ยังไม่สามารถเปิดรับอาสาสมัครได้ เนื่องจากยังไม่มีการผ่าน อย.และกระบวนการจริยธรรมการวิจัยในมนุษย์ แต่เบื้องต้นผู้ที่จะเป็นอาสาสมัครได้จะต้องมีร่างกายที่แข็งแรง และเข้าได้กับเกณฑ์การตรวจร่างกายที่กำหนด